 El carbono se define como un elemento que posee 4 electrones de valencia libre, estos les posibilitan la unión a otros a crear un compuesto en específico. Con eso se crean diversos productos químicos orgánicos dentro de la naturaleza.
El carbono se define como un elemento que posee 4 electrones de valencia libre, estos les posibilitan la unión a otros a crear un compuesto en específico. Con eso se crean diversos productos químicos orgánicos dentro de la naturaleza.
La estructura del carbono es muy diversa. Desde uno que se liga a 4 hidrógenos como el metano (CH4), hasta llegar a cadenas largas de carbono unificadas al hidrógeno tales como el n-nonano (C9H20) y también cadenas de carbono que se ligan a grupos funcionales, dentro de los cuales se destaca el etilenglicol (C2H6O2).
Existen numerosos productos químicos orgánicos que están presentes en la naturaleza y son el resultado de la complejidad de la estructura del carbono que posee cuatro electrones de valencia libre. Estos se ligan a otros átomos posibilitando la creación de compuestos numerosos.
Indice
Configuración Electrónica de un Átomo de Carbono
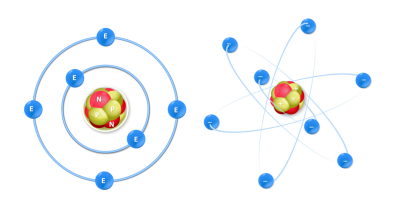 El carbono forma parte del grupo 4 y período 2 en la tabla periódica. Su número atómico (Z) está en 6, por lo tanto, su núcleo se compone de 6 neutrones, 6 protones y 6 electrones en cada una de sus órbitas.
El carbono forma parte del grupo 4 y período 2 en la tabla periódica. Su número atómico (Z) está en 6, por lo tanto, su núcleo se compone de 6 neutrones, 6 protones y 6 electrones en cada una de sus órbitas.
Estos están distribuidos en pares en los niveles correspondientes a 1s, 2s y 2p. Su número de masa es igual a 12. La configuración electrónica del carbono presente en un estado de mínima energía, también llamada basal es igual a 1s 22s23s2. Por esta razón, se compone de seis electrones en total.
Hidratación del Carbono
La hidratación del carbono está basada de manera específica en la reorganización de los electrones que forman parte de la órbita s hasta la órbita del nivel similar de energía. Cuando los enlaces son creados, los orbitales del agua se encargan de explicar la manera en la cual se localizarán cada uno de los electrones, siguiendo al pie de la letra la teoría de los enlaces de valencia.
Tipos de Hibridación del Carbono
Hibridación sp
Esta hibridación es producida a causa de la combinación de un orbital tipo p y un orbital tipo s, el resultado son dos orbitales de clase híbrida. De igual manera se liberan dos suborbitales p que se ubican de forma perpendicular a los dos orbitales de tipo híbrido sp.
Hibridación sp2
En esta clase de hibridación, luego del estado excitado se hace la combinación de dos orbitales p con un orbital s. El resultado que se obtiene son tres orbitales sp2, quedando disponible un suborbital p.
Hibridación sp3
Existe un estado intermedio al que se le llama estado excitado, este produce la hibridación sp3. Esto quiere decir que un electrón que pertenece al orbital s2 se mueve o se promueve al suborbital p que se encuentra vacío. Al final se hace una combinación del orbital 2s junto a los tres orbitales p para permitir cuatro orbitales híbridos sp3.
Usos del Carbono
- En medicina, las conocidas píldoras de carbono se usan para la absorción de toxinas en el sistema digestivo.
- Se usa para fabricar barras de acero y proteger reactores nucleares.
- La fibra de carbono se distingue como un polímero creado por grafito que se aplica en piezas de autobuses espaciales, aviones, cañas de pescar y raquetas de tenis.
- El carbón activado se usa en sistemas de purificación y filtración de agua.
Estudios y Propiedades acerca de la Configuración Electrónica del Carbono
- Los fullerenos se definen como moléculas de forma esférica creadas únicamente por átomos de carbono que sirven a una generación nueva de lubricantes. Al estar en temperaturas de 10 K y 40 K, tienen un comportamiento de súper conducción.
- En medicina, existe un metano follonero que ejerce inhibición a la proteasa del virus del SIDA, permitiendo prolongar la vida de los afectados por esta enfermedad.
- Las propiedades estructurales y químicas de los nanotubos y los géneros de carbono tratan sobre arreglos de átomos de carbono en los que sus tamaños son apenas nanómetros.

